Już 24 sierpnia 2021 roku Cara Therapeutics i jej partner biznesowy Vifor Pharma ogłosili, że ich pierwszy w swojej klasie agonista receptora opioidowego kappa, difelikefalina (KORSUVA™), został zatwierdzony przez FDA do leczenia pacjentów z przewlekłą chorobą nerek (PChN) (z umiarkowanym/ciężkim świądem u pacjentów poddawanych hemodializie). Jego wprowadzenie na rynek planowane jest na pierwszy kwartał 2022 roku. Cara i Vifor podpisały umowę licencyjną na wyłączność na komercjalizację KORSUVA™ w Stanach Zjednoczonych i zgodziły się sprzedać KORSUVA™ firmie Fresenius Medical. Firmy te mają odpowiednio 60% i 40% udziału w przychodach ze sprzedaży poza Fresenius Medical; każda z nich ma 50% udziału w przychodach ze sprzedaży od Fresenius Medical.
Świąd związany z PChN (CKD-aP) to uogólniony świąd, który występuje z dużą częstością i intensywnością u pacjentów z PChN poddawanych dializie. Świąd występuje u około 60–70% pacjentów dializowanych, z czego 30–40% ma umiarkowany/ciężki świąd, który poważnie wpływa na jakość życia (np. pogarsza jakość snu) i jest związany z depresją. Dotychczas nie było skutecznego leczenia świądu związanego z PChN, a zatwierdzenie leku Difelikefalin pomaga wypełnić ogromną lukę w potrzebach medycznych. Zatwierdzenie to opiera się na dwóch kluczowych badaniach klinicznych fazy III, zgłoszonych w ramach wniosku o dopuszczenie do obrotu (NDA): pozytywnych danych z badań KALM-1 i KALM-2 w USA i na świecie oraz danych uzupełniających z 32 dodatkowych badań klinicznych, które wykazują dobrą tolerancję leku KORSUVA™.
Niedawno pojawiły się dobre wieści z badania klinicznego difelikefaliny w Japonii: 10 stycznia 2022 r. firma Cara ogłosiła, że jej partnerzy, Maruishi Pharma i Kissey Pharma, potwierdzili, że wstrzyknięcia difelikefaliny są stosowane w Japonii w leczeniu świądu u pacjentów hemodializowanych. Badania kliniczne fazy III. Pierwszorzędowy punkt końcowy został osiągnięty. 178 pacjentów otrzymywało difelikefalinę lub placebo przez 6 tygodni i uczestniczyło w 52-tygodniowym otwartym badaniu przedłużonym. Pierwszorzędowy punkt końcowy (zmiana wyniku w numerycznej skali oceny świądu) i drugorzędowy punkt końcowy (zmiana wyniku w skali nasilenia świądu Shiratori) uległy istotnej poprawie w porównaniu z wartościami wyjściowymi w grupie difelikefaliny w porównaniu z grupą placebo i były dobrze tolerowane.
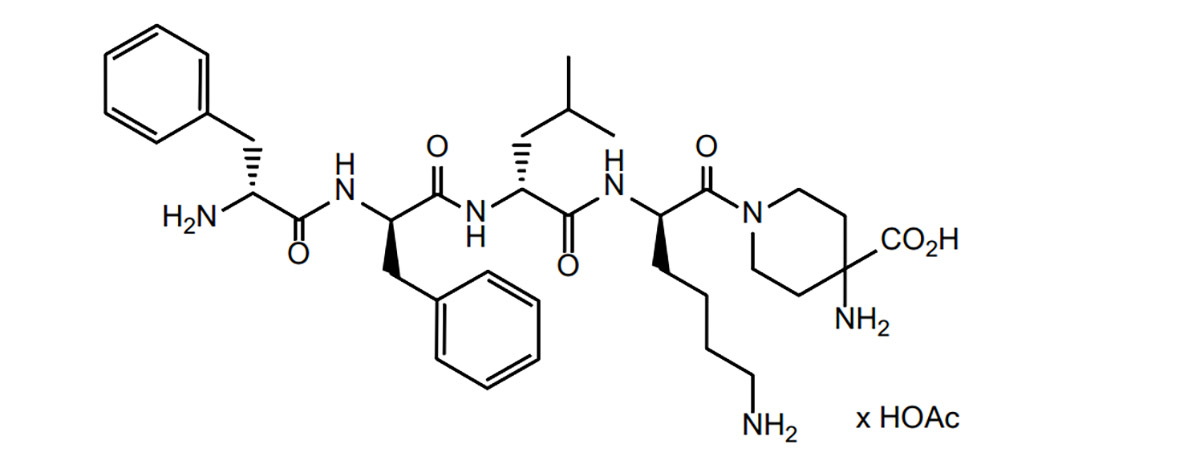
Difelikefalina to klasa peptydów opioidowych. Na tej podstawie Instytut Badań nad Peptydami przeanalizował literaturę dotyczącą peptydów opioidowych i podsumował trudności oraz strategie związane z peptydami opioidowymi w rozwoju leków, a także obecną sytuację w tym zakresie.
Czas publikacji: 17 lutego 2022 r.